安徽华源医药股份有限公司
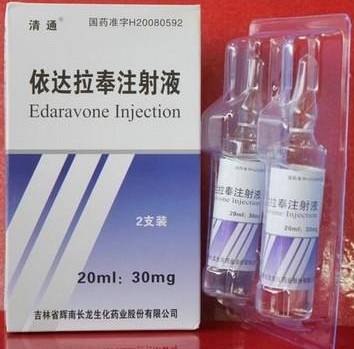
| 包装规格:20ml:30mg | |
| 招商区域:全国 全国各地区 | |
| 销售渠道:OTC | |
| 批准文号:001170206 | |
| 主要成份:本品主要成份为依达拉奉。 辅抖:亚硫酸氢钠、L-盐酸半胱氨酸-水合物、氯化钠、注射用水。 |
|
| 点击次数:7940 | |
| 更新时间: 2024-10-17 10:40:33 | |
| 给厂家留言,让厂家主动联系你 | |
| 包装规格:20ml:30mg | 销售渠道:OTC | 招商区域:全国全国各地区 |
产品功效:依达拉奉注射液,用于改善急性脑梗塞所致的神经症状、日常生活活动能力和功能障碍
用法用量:据日本临床病例569例观察,26例(4.57%)出现不良反应。主要表现为肝功能异常16例(2. 81%),皮疹4例(0.70%)。569例中临床检测值异常变化的有122例(21.4%),主要是AST上升 7.71%(43/558,ALT上升8.23%(45/559)等肝功能检测值异常。
严重不良反应有:
1、急性肾功能衰竭(程度不明) 用药过程中进行多次肾功能检测并密切观察,出现肾功能低下表现或少尿等症状时,停止用药并正确处理。
2、肝功能异常、黄疸(均程度不明) 伴有AST、ALT、ALP、Y-GTP、LDH上升等肝功能异常和黄疸,用药过程中需检测肝功能并密切观察,出现异常情况,停止用药并正确处理。
3、血小板减少{程度不明) 有血小板减少表现,用药过程中需密切观察,出现异常情况,停止给药并正确处理。
4、弥漫性血管内凝血(DIC)(程度不明) 可出现弥漫性血管内凝血的表现,用药过程中定期检测,出现疑为弥漫性血管内凝血的实验室表现和临床症状时,停止给药并进行正确处理。
其他不良反应(发生率)及主要表现为:
1、过敏症(0.1-5%):主要表现为皮疹、潮红、肿胀、疱疹、搔痒感;
2、血细胞系统(0.1-5%):主要表现为红细胞减少,白细胞增多,白细胞减少,红细胞压积值减少,血红蛋白减少,血小板增多,血小板减少;
3、注射部位(0.1-5%):主要表现为注射部位皮疹、红肿;
4、肝脏(发生率>5%):土要表现为AST升高,ALT升高,LDH升高,ALP升高,Y -GTP升高;
5、肾脏(0.1-5%):主要表现为BUN升高,血清尿酸升高,血清尿酸下降,蛋白尿、血尿、肌酐升高(程度不明);
6、消化系统(0.1-5%):嗳气。
7、其他(0.1-5%):发热、热感,血压升高,血清胆固醇升高,血清胆固醇降低,甘油三酯升高,血清总蛋白减少,CK(CPK)升高,CK(CPK)降低,血清钾下降,血清钙下降。
用法用量:据日本临床病例569例观察,26例(4.57%)出现不良反应。主要表现为肝功能异常16例(2. 81%),皮疹4例(0.70%)。569例中临床检测值异常变化的有122例(21.4%),主要是AST上升 7.71%(43/558,ALT上升8.23%(45/559)等肝功能检测值异常。
严重不良反应有:
1、急性肾功能衰竭(程度不明) 用药过程中进行多次肾功能检测并密切观察,出现肾功能低下表现或少尿等症状时,停止用药并正确处理。
2、肝功能异常、黄疸(均程度不明) 伴有AST、ALT、ALP、Y-GTP、LDH上升等肝功能异常和黄疸,用药过程中需检测肝功能并密切观察,出现异常情况,停止用药并正确处理。
3、血小板减少{程度不明) 有血小板减少表现,用药过程中需密切观察,出现异常情况,停止给药并正确处理。
4、弥漫性血管内凝血(DIC)(程度不明) 可出现弥漫性血管内凝血的表现,用药过程中定期检测,出现疑为弥漫性血管内凝血的实验室表现和临床症状时,停止给药并进行正确处理。
其他不良反应(发生率)及主要表现为:
1、过敏症(0.1-5%):主要表现为皮疹、潮红、肿胀、疱疹、搔痒感;
2、血细胞系统(0.1-5%):主要表现为红细胞减少,白细胞增多,白细胞减少,红细胞压积值减少,血红蛋白减少,血小板增多,血小板减少;
3、注射部位(0.1-5%):主要表现为注射部位皮疹、红肿;
4、肝脏(发生率>5%):土要表现为AST升高,ALT升高,LDH升高,ALP升高,Y -GTP升高;
5、肾脏(0.1-5%):主要表现为BUN升高,血清尿酸升高,血清尿酸下降,蛋白尿、血尿、肌酐升高(程度不明);
6、消化系统(0.1-5%):嗳气。
7、其他(0.1-5%):发热、热感,血压升高,血清胆固醇升高,血清胆固醇降低,甘油三酯升高,血清总蛋白减少,CK(CPK)升高,CK(CPK)降低,血清钾下降,血清钙下降。